وفقا لدراسة نشرت فيخلية،طور الباحثون مثبطًا محددًا لـ KRASG12C يسمى ARS-1602، والذي أدى إلى تراجع الورم في الفئران.
"توفر هذه الدراسة أدلة حية على أن طفرة KRAS يمكن استهدافها بشكل انتقائي، وتكشف عن ARS-1620 باعتباره يمثل جيلًا جديدًا من مثبطات KRASG12C المحددة مع إمكانات علاجية واعدة"، كما أشار المؤلف الرئيسي، ماثيو آر جينس، دكتوراه، من Wellspring Biosciences في سان دييغو، كاليفورنيا، وزملاؤه.
طفرات KRAS هي الجينات المسرطنة الأكثر شيوعًا وقد أظهرت الأبحاث السابقة أن حوالي 30٪ من الأورام تحتوي على طفرات RAS. تهيمن طفرات KRAS المحددة ضمن أنواع محددة من الأورام. على سبيل المثال، KRASG12C هو طفرة سائدة في سرطان الرئة ذو الخلايا غير الصغيرة (NSCLC)، ويوجد أيضًا في الأورام الغدية البنكرياسية والقولونية والمستقيم.
على الرغم من انتشار وعقود من الأبحاث التي تسلط الضوء على KRAS المتحول كمحرك رئيسي لتكوين الأورام والمقاومة السريرية، إلا أن KRAS المتحول كان هدفًا عنيدًا.
حاولت مجموعة متنوعة من الاستراتيجيات تحديد الجزيئات الصغيرة التي تستهدف KRAS، لكنها أدت إلى قمع محدود لـ KRAS في الخلايا. وقد حفز هذا المؤلفين على تصميم مركب لتحسين مثبطات KRAS المحددة، بما في ذلك مثبطات KRASG12C لجيب المفتاح 2 (S-IIP)، التي ترتبط بحالة KRAS المرتبطة بالناتج المحلي الإجمالي وتتفاعل معها، مما يؤدي إلى احتجازها في شكل غير نشط.
لكي يكون فعالا، يجب أن يكون للمثبط قوة عالية وحركية ربط سريعة. يجب أن يتمتع أيضًا بخصائص حركية دوائية مثالية للحفاظ على التعرض والمدة لفترة طويلة بما يكفي لالتقاط الحالة غير النشطة المرتبطة بالناتج المحلي الإجمالي لـ KRAS والتي تمر بدورة نيوكليوتيدات سريعة.
قام الباحثون بتصميم وتصنيع ARS-1620 بخصائص شبيهة بالعقاقير، وتحسين فعاليته مقارنة بمركبات الجيل الأول. تم بعد ذلك تقييم الفعالية والحركية عبر خطوط الخلايا مع الأليل الطافر لتحديد ما إذا كان الإشغال المستهدف لتثبيط KRAS-GTP في الأورام كافيًا.
تم تقييم تثبيط نمو الخلايا، فضلا عن إمكانية حدوث تفاعلات غير محددة يمكن أن تشير إلى احتمال التسمم.
أخيرًا، لتقييم الإشغال المستهدف في الجسم الحي، تم إعطاء ARS-1620 عن طريق الفم للفئران التي لديها نماذج طعم أجنبي تحت الجلد تحمل KRAS p.G12C كجرعة وحيدة، أو يوميًا لمدة 5 أيام.
أفاد الباحثون أن ARS-1620 يمنع بشكل كبير نمو الورم بطريقة تعتمد على الجرعة والوقت مع تراجع ملحوظ للورم.
في خمسة نماذج طعم أجنبي لخطوط الخلايا NSCLC في الفئران، استجابت جميع النماذج بعد أسبوعين إلى ثلاثة أسابيع من العلاج، وأظهرت أربعة من الخمسة قمعًا كبيرًا لنمو الورم. بالإضافة إلى ذلك، تم تحمل ARS-1620 جيدًا دون أي سمية سريرية ملحوظة خلال فترة العلاج.
"بشكل جماعي، فإن الأدلة الحية على أن ARS-1620 فعال على نطاق واسع كعامل واحد عبر نماذج NSCLC توفر دليلاً على مفهوم أن جزءًا كبيرًا من المرضى الذين يعانون من طفرات p.G12C KRAS قد يستفيدون من العلاجات الموجهة بـ KRASG12C"، حسبما ذكر المؤلفون.
وأضافوا أن ARS-1620 هو مثبط مباشر للجزيء الصغير KRASG12C، وهو قوي وانتقائي ومتوفر بيولوجيًا عن طريق الفم وجيد التحمل.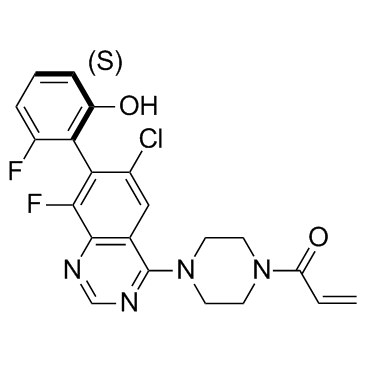
وقت النشر: 22 مايو 2018
