Prema studiji objavljenoj ućelija,istraživači su razvili specifični inhibitor za KRASG12C nazvan ARS-1602 koji je inducirao regresiju tumora kod miševa.
„Ova studija pruža in vivo dokaze da se mutantni KRAS može selektivno ciljati i otkriva da ARS-1620 predstavlja novu generaciju inhibitora specifičnih za KRASG12C sa obećavajućim terapijskim potencijalom“, rekao je glavni autor, dr Matthew R Janes, iz Wellspring Biosciences u San Diego, CA, i kolege.
KRAS mutacije su najčešće mutirani onkogen i prethodna istraživanja su pokazala da otprilike 30% tumora sadrži RAS mutacije. Specifične KRAS mutacije dominiraju unutar specifičnih tipova tumora. Na primjer, KRASG12C je dominantna mutacija u karcinomu ne-malih stanica pluća (NSCLC), a također se nalazi u adenokarcinomima gušterače i debelog crijeva.
Uprkos rasprostranjenosti i decenijama istraživanja koja ističu mutantni KRAS kao centralni pokretač tumorigeneze i kliničke rezistencije, mutantni KRAS je bio tvrdoglava meta.
Različite strategije su pokušale identificirati male molekule koje ciljaju KRAS, ali su rezultirale ograničenom supresijom KRAS-a u stanicama. Ovo je motivisalo autore da dizajniraju jedinjenje za poboljšanje KRAS-specifičnih inhibitora, uključujući KRASG12C inhibitore prekidača 2 džepa (S-IIP) koji se vezuju za GDP-vezano stanje KRAS-a i reaguju sa njim, hvatajući ga u neaktivnu konformaciju.
Da bi bio efikasan, inhibitor mora imati visoku snagu i brzu kinetiku vezivanja. Takođe mora imati optimalna farmakokinetička svojstva kako bi održala izloženost i trajanje dovoljno dugo da uhvati GDP-vezano neaktivno stanje KRAS-a koji prolazi kroz brzi nukleotidni ciklus.
Istraživači su dizajnirali i sintetizirali ARS-1620 sa svojstvima sličnim lijekovima i poboljšanom potencijom u odnosu na spojeve prve generacije. Učinkovitost i kinetika u ćelijskim linijama s mutiranim alelom su zatim procijenjene kako bi se utvrdilo da li je ciljna zauzetost za inhibiciju KRAS-GTP u tumorima dovoljna.
Procijenjena je inhibicija rasta stanica, kao i mogućnost nespecifičnih reakcija koje bi mogle ukazivati na potencijalnu toksičnost.
Konačno, da bi se procijenila ciljna popunjenost in vivo, oralni ARS-1620 je dat miševima sa utvrđenim modelima potkožnog ksenotransplantata koji su nosili KRAS p.G12C kao pojedinačna doza ili dnevno tokom 5 dana.
Istraživači su izvijestili da ARS-1620 značajno inhibira rast tumora na način ovisan o dozi i vremenu uz izraženu regresiju tumora.
U pet modela ksenotransplantata NSCLC ćelijskih linija kod miševa, svi modeli su odgovorili nakon dvije do tri sedmice liječenja, a četiri od pet su pokazala značajnu supresiju rasta tumora. Osim toga, ARS-1620 se dobro podnosio bez uočene kliničke toksičnosti tokom perioda liječenja.
„Zajedno, in vivo dokazi da je ARS-1620 uglavnom efikasan kao pojedinačni agens u svim modelima NSCLC pruža dokaz koncepta da značajan dio pacijenata sa p.G12C KRAS mutacijama može imati koristi od terapija usmjerenih na KRASG12C,“ navode autori.
Dodali su da je ARS-1620 direktni inhibitor malih molekula KRASG12C koji je moćan, selektivan, oralno biodostupan i dobro se podnosi.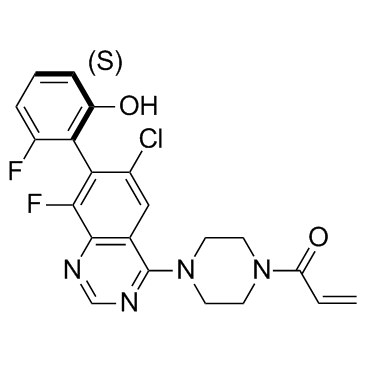
Vrijeme objave: 22.05.2018
